Wie nennt man den inneren Inhalt einer Kastanie? Gewöhnliche Rosskastanie
Es wächst natürlich auf dem Balkan. Wächst in Laubwäldern des Vorgebirges. Photophiler Mesophyt, Mesotroph. Weit verbreitet im städtischen Landschaftsbau in Europa, Zentralasien, Ostasien und Nordamerika.
Foto von Elena Bayrasheva
Ein mächtiger, bis zu 30 m hoher Baum mit massivem Stamm und schwerer, dichter, weit gerundeter Krone, auffallend großen Blütenständen und sehr dekorativen Früchten. Er genießt zu Recht den Ruf eines der schönsten Parkbäume, der das ganze Jahr über dekorativ ist: im Winter - mit einem wunderschönen Muster aus kräftigen Zweigen; im Frühling - früh blühende, große, klebrige, grünlich-rosa Knospen, aus denen an einem der warmen Tage ursprüngliche, faltige, komplexe, langblättrige Blätter hervorgehen, die bei voller Entwicklung einen dichten Schatten spenden. Die Blätter sind zusammengesetzt, handförmig, mit 5-7 länglichen, verkehrt eiförmigen Blättchen mit einer Länge von bis zu 25 cm. Anfang Mai, nach der Blattblüte, erscheinen große (bis zu 30 cm) pyramidenförmige Rispen mit großen, weißen, rosa gesprenkelten Blüten . Wie Kerzen an einem Weihnachtsbaum verleihen die Blütenstände dem Baum in dieser Zeit ein einzigartiges Aussehen. Die Blüte dauert 15-25 Tage. Auch Kastanienfrüchte sind sehr dekorativ – kugelförmig, grün, mit zahlreichen Dornen, fleischige Kapseln mit bis zu 6 cm Durchmesser, rissig mit drei Blättern und enthalten 1-3 glänzende, dunkelbraune Samen.
Frostbeständig, hohe Ansprüche an die Bodenfruchtbarkeit, bevorzugt kalkhaltigen Lehm. Schattentolerant, aber bessere Entwicklung reicht auf offen sonnige Orte. Es stellt hohe Ansprüche an die Boden- und Luftfeuchtigkeit, verträgt städtische Bedingungen relativ gut und hat eine hohe Fähigkeit, Schwefelverbindungen und Blei anzureichern. Resistent gegen Schädlinge und Krankheiten. Behält seine dekorativen Eigenschaften lange Zeit. Sehr farbenfroh im Herbst, wenn sich das Laub in ein wunderschönes leuchtendes Gelb färbt. Eine gute Honigpflanze. Dauerhaft.
Ein erstklassiger Baum zur Bepflanzung von Straßen, Boulevards und Parkalleen. Es eignet sich auch gut für monumentale Gruppen und ganze Haine in großen Parks und Waldparks. Sehr schön in einer Einzelpflanzung, bei der die Krone die Möglichkeit hat, sich voll zu entwickeln. In der Kultur seit 1576.
In GBS wurden seit 1941 5 Proben (22 Exemplare) aus Samen verschiedener botanischer Gärten gezüchtet. Mit 61 Jahren beträgt die Höhe 13 m, der Stammdurchmesser 23 cm und wächst vom dritten Zehntag im April bis zum zweiten Zehntag im Oktober. Es wächst langsam. Sie blüht ab einem Alter von 9 Jahren, von der dritten Maidekade bis zur zweiten Junidekade. Sie trägt ab dem 9. Lebensjahr Früchte, die Früchte reifen in der zweiten Septemberhälfte. Die Winterhärte ist hoch. Die Lebensfähigkeit der Samen beträgt 100 %, die Keimfähigkeit ist durchschnittlich. Eine Vermehrung durch Pfropfen ist möglich. Empfohlen für die Landschaftsgestaltung in Moskau für Allee-, Gruppen- und Einzelbepflanzungen.
Bei der Lagerung von Saatgut ist darauf zu achten, dass die Luftfeuchtigkeit (ca. 40 %) und die Temperatur zwischen 0 und 5 °C liegen. Stratifizieren Sie die Samen vor der Aussaat in Sand bei Temperaturen bis 10 °C für 2 – 5 Monate (abhängig von den Lagerbedingungen). Normalerweise werden die Samen spätestens im nächsten Frühjahr nach der Ernte ausgesät. Saattiefe 6 - 10 cm.
 Foto von Olga Blokhman
Foto von Olga Blokhman
Es gibt eine Reihe dekorativer Formen: Baumann(f. Baumanii) – mit gefüllten weißen Blüten und langer Blüte, bringt keine Früchte hervor; Schirnhofera (f. Schimhoferi) – mit gefüllten gelblich-roten Blüten; gelb-bunt(f. luteo-variegata) – mit gelb-bunten Blättern; weiß-weiß(f. albo-variegata) – mit weiß-bunten Blättern; Memminger(f. Memmingeri) – kleine weiße Flecken auf den Blättern; gespalten(f. laciniata) – mit schmalen, stark ungleichmäßig geschnittenen Blättern; schirmförmig(f. umbraculifera) – mit kompakter, abgerundeter Krone; Pyramidenförmig (f. Pyramidalis) – mit schmaler Pyramidenkrone; unterdimensioniert(f. pumila) - Zwerg; ausgeschnitten(f. incisa) – mit kurzen und breiten, tief eingeschnittenen Blättern; Weinen(f. Pendel).
"Baumannii„Die Form des Baumes ist konvex oder breit eiförmig, 15–20 m hoch, 8–12 m breit, kompakt im Aussehen, nicht so groß wie die ursprüngliche Art. Blüten – große Ähren, weiß, mit rotem Muster, Blüten ( ab dem 10. Jahr) von Anfang bis Mitte Mai. Früchte fehlen fast vollständig. Blätter sind schön, groß, bis zu 25 cm, länglich-elliptisch oder lanzettlich, narbig handförmig, oft mit sichelförmigen Zähnen; im Herbst hell gelb. Wurzelsystem: oberflächlich und verzweigt, empfindlich gegenüber Bodenverdichtung und Eingriffen; hebt sich Straßenoberflächen. Bevorzugt warme Standorte, ist frostbeständig und empfindlich gegenüber trockener Luft. Die Böden sind feucht bis feucht, leicht sauer bis alkalisch; leicht schwere Böden; wächst nicht weiter sandige Böden; empfindlich gegenüber Salzgehalt. Frostbeständigkeit: Zone 4.
Familie der Rosskastanien, Gattung der Rosskastanien. Die Gewöhnliche Rosskastanie ist ein Baum, sie wird auch als anmutig bezeichnet, da der Stamm die richtige Form hat. Auch für medizinische Zwecke weit verbreitet. Erstens handelt es sich um einen Laubbaum aus der Familie der Rosskastanien. Je nach Wachstumsbedingungen wird es bis zu 30–35 Meter oder mehr groß.
Gewöhnliche Rosskastanie - Beschreibung, Foto und Video
Es hat eine große und ausladende Krone, die sich beim leisesten Windhauch majestätisch wiegt. Frisch erblühte Triebe sind entweder graubraun oder rotbraun. Die Blätter haben andere Form, aber im Grunde handelt es sich um eine fingerkomplexe Form. Die Blüten sind fast immer blassrosa oder weiß und in kegelförmigen Blütenständen gesammelt.
Die Frucht ist eine kleine Kapsel, innen ist sie mit Samen gefüllt und außen mit Dornen bedeckt. Dieser Baum wurde vor allem deshalb so genannt, weil nach dem Laubfall eine Narbe auf der Rinde zurückbleibt, die dem Hufeisen eines Pferdes sehr ähnlich ist. Dieser Baum blüht im Mai oder Juni und die Früchte reifen Ende August, Anfang September.
Gewöhnliche Rosskastanie – unter natürlichen Bedingungen im Norden Indiens zu finden, Südeuropa, Ostasien und Nordamerika. Übrigens gilt es zu Recht als Heimat Nordamerika Hier kommen die meisten Arten dieses schönen Baumes vor.
Er wächst bevorzugt in der gemäßigten Zone, wo das Klima für diesen Baum am besten geeignet ist, und liebt außerdem fruchtbaren und frischen Boden. Wächst auch in Berggebieten, Balkanhalbinsel, dort wird es in großen Mengen verteilt. In der europäischen Kultur wird es schon seit sehr langer Zeit, genauer gesagt seit dem 16. Jahrhundert, verwendet.
Dieser Typ wird häufig für medizinische Zwecke verwendet. Vor nicht allzu langer Zeit untersuchten Wissenschaftler speziell verschiedene Alkoholtinkturen, Abkochungen und dergleichen, speziell aus diesem Baum und seinen Bestandteilen. Und sie kamen zu dem Schluss, dass der Alkoholextrakt der Frucht für medizinische Zwecke am wirksamsten ist. Dieser Extrakt enthält viele Substanzen wie Aescin, Aesculin und Glykoside.
 Extrakte dieser Art erhöhen den Tonus der Venengefäße und beschleunigen zudem den Blutfluss in den Venen. Dies verhindert die Entstehung eines Phänomens wie einer Thrombose. Darüber hinaus haben Präparate aus den Bestandteilen dieses Baumes entzündungshemmende Eigenschaften. Auch Tinkturen aus Blüten, Rinde oder Blättern werden schon seit längerem verwendet Volksmedizin.
Extrakte dieser Art erhöhen den Tonus der Venengefäße und beschleunigen zudem den Blutfluss in den Venen. Dies verhindert die Entstehung eines Phänomens wie einer Thrombose. Darüber hinaus haben Präparate aus den Bestandteilen dieses Baumes entzündungshemmende Eigenschaften. Auch Tinkturen aus Blüten, Rinde oder Blättern werden schon seit längerem verwendet Volksmedizin.
Solche Tinkturen helfen bei Rheuma, Venenerkrankungen und verschiedenen Magenerkrankungen. Es ist jedoch anzumerken, dass für die Zubereitung solcher Tinkturen kein großer Bedarf besteht. Denn aus den Bestandteilen dieses Baumes kann man in der Apotheke jedes Medikament kaufen.
Von recht großer wirtschaftlicher Bedeutung ist beispielsweise die Gewöhnliche Rosskastanie, von der es viele gibt Gartenformen, die sich in der Form von Blättern, Kronen usw. unterscheiden. In Russland wird sie seit geraumer Zeit als Landschaftspflanze verwendet und in Parks, Gärten und auf Plätzen gepflanzt.
In Russland kann es jedoch nur in südlichen Städten wachsen, da es ein warmes Klima liebt. Holz ist weich und lässt sich leicht streichen. verschiedene Farben, und wird auch beim Drehen und verwendet Zimmerei. Die Früchte werden als Futter für Tiere wie Schafe und Schweine verwendet. Es gibt eine interessante Tatsache, die von Stockholmer Wissenschaftlern herausgefunden wurde: Der springende Punkt ist, dass ein solcher Baum etwa 20.000 Kubikmeter Luft von schädlichen Abgasen reinigen kann.
Deshalb wird es in großem Umfang im Gartenbau eingesetzt. Diese Art ist auch eine ausgezeichnete Honigpflanze; während der Blüte produziert sie Honig große Menge Pollen und Nektar. Der Nektar dieses Baumes enthält 60-70 % Zucker. Honig ist auch einzigartig, er ist transparent und zähflüssig und hat normalerweise überhaupt keine Farbe.
Sehen Sie sich das Video Rosskastanie an
Wie schön die Kastanienblüten sind! Seine Blumen leuchten wie Kerzen und die Luft um dich herum scheint zu glühen.
An den Hängen des Hauptkaukasusgebirges wachsen echte Kastanien oder Samenkastanien. Aber Sie können die falsche oder Rosskastanie auch in bewundern mittlere Spur. Dieser bis zu 30 Meter hohe Baum ist nicht nur für seine Schönheit berühmt. Es gibt den Menschen Gesundheit.
Rosskastanienblätter werden in der Medizin in den USA seit langem als Vitamin-K-Quelle verwendet. Daraus hergestellte Zubereitungen werden in unserem Land auch als Stärkungsmittel verwendet. Die Rinde und Früchte helfen bei chronischen Erkrankungen des Magen-Darm-Traktes, Hämorrhoiden. Arteriosklerose und Thrombophlebitis werden mit Extrakt aus der Rinde behandelt. Pollen werden zur Behandlung von Prostatitis und Krampfadern als Mittel zur Regulierung eingesetzt arterieller Druck, was die Blutzusammensetzung verbessert. In Aserbaidschan ein Aufguss aus Kastanienfrüchten Wassermelonensaft Getränk gegen Malaria.

Aus Kastanienfrüchten wurden besonders wertvolle und heilkräftige Biersorten hergestellt, beispielsweise das Königsbier. Für drei Liter Wasser nehmen Sie 10-20 (je nach Größe) geschälte Rosskastanienfrüchte. Sie müssen halbiert werden, aber nicht kleiner, sonst wird das Getränk bitter. Geben Sie die gehackten Kastanien in einen Beutel mit Locher, geben Sie sie in ein Glas und fügen Sie 1 Tasse Zucker und 1 Teelöffel Sauerrahm hinzu. Mit drei Lagen Gaze abdecken und an einen dunklen, warmen Ort stellen. Die Gärung dauert zwei Wochen, danach erhält man ein sehr angenehm schäumendes Getränk. Es entfernt nicht nur schnell Radionuklide aus dem Körper, sondern liefert auch Kalzium, Kupfer, Kobalt und Jod. Sie sollten dieses Bier einen Monat lang dreimal täglich, ein halbes Glas oder so viel Sie möchten, 15-20 Minuten vor den Mahlzeiten trinken. Die der Abnahme entsprechende Menge Wasser und Zucker wird täglich zugegeben.
 (Rosskastanie)
(Rosskastanie) Das Getränk ist auch für Kinder ab einem Jahr geeignet. Es heilt den Körper und ermöglicht es Ihnen, viele Krankheiten loszuwerden. Die Praxis zeigt, dass dies ein wahres Jugendelixier ist, das die Haarfarbe teilweise wiederherstellt und verbessert allgemeiner Zustand. Nur nicht vergessen mit Süßwasser Fügen Sie regelmäßig Kastanien hinzu – dann ist das Bier mehrere Monate haltbar. (Zoya Kovalenko, Moskau).

Gewöhnliche Rosskastanie(lat. Aesculus hippocastanum) ist ein großer Laubbaum, die bekannteste Art der Rosskastaniengattung in Russland. Wächst weiter kleiner Bereich in den Bergen des Balkans (im Norden Griechenlands, Albaniens, der Republik Mazedonien, Serbien und Bulgarien) in Laubwäldern zusammen mit Erle, Esche, Ahorn, Hainbuche, Linde, Buche und anderen Baumarten, die bis in die Berge reichen eine Höhe von 1000-1200 m über dem Meeresspiegel. Es kommt in den Bergregionen Irans und in den Ausläufern des Himalaya vor. In der gemäßigten Klimazone weit verbreitet angebaut, häufig in Anpflanzungen in vielen Regionen des europäischen Teils Russlands.
Langlebig (erreicht unter günstigen Bedingungen ein Alter von 200-300 Jahren). Nahezu nicht durch Insekten beschädigt. Verträgt eine Transplantation im Erwachsenenalter gut.
Schattentolerant, wächst gut auf tiefen, lockeren Böden - Ton oder sandiger Lehm, ausreichend feucht, aber ohne übermäßige Feuchtigkeit. Verträgt ziemlich trockenes Wetter Chernozem-Böden In der Steppenzone verträgt es salzhaltige Böden nicht gut. Empfindlich gegenüber trockenem Wind, weshalb die Blätter im Sommer oft stark verbrennen und vorzeitig abfallen.
Winterhart im Anbau in der zentralen Zone des europäischen Teils Russlands (bis Moskau). Auf dem Breitengrad von Moskau friert es in sehr strengen Wintern; Auch in St. Petersburg frieren junge Bäume ein, aber an geschützten Orten wachsen sie zu großen, üppig blühenden Bäumen heran.
Verwendete Materialien:
- Z. Kovalenko.
Rosskastanie, häufigAesculus hippocastanum L. Rosskastanie, häufig- Laubbaum aus der Familie der Rosskastanien Hippocastanoideae. Ein ziemlich großer Laubbaum, der eine Höhe von 30 bis 15 Metern und einen Umfang von bis zu 2 Metern erreicht. Mit großen, klebrigen Knospen und einer dichten, breiten, meist runden oder pyramidenförmigen Krone. Die Blätter sind bis zu 20 cm lang und 10 cm breit, an langen Blattstielen etwa 15–20 cm. Sie bestehen aus 5–7 großen, sitzenden Blattplatten, mit größeren in der Mitte und kleineren äußeren. Die Blattspreiten sind verkehrt eiförmig oder länglich, zur Basis hin schmaler, spitz zulaufend und an den Rändern ungleichmäßig gesägt. MIT Rückseite kahl, Oberseite mit weichen Haaren. Die Blüten haben 5 Blütenblätter, rund, an den Rändern schuppig, weiß, mit gelber Fleck an der Basis, die sich später rosa verfärbt. In geraden, dichten Rispen von bis zu 20-30 cm Länge angeordnet, Stecklinge und Stiele rotbraun behaart. Der Kelch ist zylindrisch und glockenförmig, kurz weichhaarig, die Staubblätter sind an der Basis behaart. Die Blüten sind bisexuell (es gibt sowohl männliche als auch männliche). weibliche Organe), werden von Bienen bestäubt. Der Eierstock ist mit weichen Haaren und Stacheln bedeckt. Die Früchte sind runde grüne Kapseln mit 3-4 Stacheln an jeder Rispe, meist mit einem (selten zwei oder drei) großen nussförmigen Samen von 2 bis 4 cm Durchmesser. Wenn die Kapseln reifen, nehmen sie eine bräunliche Farbe an, die Stacheln werden gröber, woraufhin die Kapseln abfallen und sich öffnen, wodurch der Samen freigesetzt wird. Der Samen hat eine glänzende braune Kruste mit einem großen weißlichen Fleck, der sich in einer separaten Schicht ablösen kann. Im Inneren ist der Samen weich, gelblich-weiß, hat 2 große, fleischige, fettige und stärkehaltige Keimblätter, die oft entlang einer Nahtlinie mehr oder weniger auffällig verwachsen sind. Sie blüht im Mai, Früchte und Samen reifen im August-September. Wenn es wild wächst, wird es durch Samen vermehrt. |
Rosskastanie, häufig- eine einheimische Pflanze in Westasien, die derzeit in vielen Ländern der Welt, in der Ukraine (Kiew) sowie in Europa und den Vereinigten Staaten von Amerika in Parks, Gärten und entlang von Stadtstraßen angebaut wird. Rosskastanienblüten haben einen zarten Honigduft. Die Gewöhnliche Rosskastanie wird oft einfach „Rosskastanie“ genannt, sie muss jedoch von anderen Mitgliedern der Gattung Rosskastanie unterschieden werden.
Die Rosskastanie wächst bevorzugt auf tiefgründigen, lehmigen und gut durchlässigen Böden. Ein sehr dekorativer und schnell wachsender Baum, der als sehr winterhart gilt. Allerdings neigt er dazu, plötzlich alte, schwere Äste abzuwerfen, weshalb er beschnitten werden muss. Der Rosskastanienbaum (gemeiner Baum) beginnt 20 Jahre nach der Aussaat der Samen Früchte zu tragen.
Die Samen keimen sehr schnell und müssen vor rauen Wetterbedingungen geschützt werden. Das Saatgut hat eine sehr begrenzte Keimfähigkeit und sollte nicht austrocknen. Gelagerte Rosskastaniensamen sollten vor der Aussaat 24 Stunden lang eingeweicht werden. Am besten säen Sie die Samen mit dem weißen Fleck nach unten.
AUFMERKSAMKEIT! Rosskastaniensamen enthalten giftige Saponine, die ihnen einen bitteren Geschmack verleihen. Sie sind für den Menschen giftig, daher ist der Verzehr roher Kastanien streng kontraindiziert.
Saponine sind auch giftig für Fische, und die Jägerstämme der amerikanischen Ureinwohner legten traditionell große Mengen Kastaniensamen in Bäche, Seen und andere Gewässer, um Fische zu betäuben oder zu töten. Einige Säugetiere, wie zum Beispiel Hirsche, können Kastanienfrüchte ohne Schaden fressen. Es sind Fälle bekannt, in denen die Früchte der Rosskastanie (gewöhnlich) als Viehfutter verwendet werden.
Kontraindikationen
Individuelle Unverträglichkeiten, Allergien. Seien Sie vorsichtig mit der Dosierung. Schwangerschaft und Stillzeit – nur nach Rücksprache mit einem Arzt. Für Menschen mit Nieren- oder Lebererkrankungen wird der Verzehr von Rosskastaniensamen auch nach der Verarbeitung nicht empfohlen.
Rosskastanienpräparate sind bei einer Allergie gegen Pflanzen der Familie der Rosskastanien kontraindiziert Hippocastanoideae.
Trotz der Tatsache, dass es sie gibt beliebte Empfehlungen zur Anwendung von Rosskastanie (gewöhnlich) bei Mastitis (Säuglinge) – Präparate aus Rosskastanie (gewöhnlich) sollten während der Schwangerschaft und Stillzeit nicht ohne ärztliche Verschreibung und Aufsicht angewendet werden.
Nebenwirkungen: in manchen Fällen werden Magen-Darm-Beschwerden wie Übelkeit und Magenbeschwerden beobachtet. Auch allergische Reaktionen sind möglich.
Die Verwendung von Rosskastanie (gewöhnlich) beim Kochen
Geröstete Samen werden als Kaffeeersatz verwendet. Allerdings müssen vor dem Verzehr giftige Saponine aus den Samen entfernt werden – durch diesen Prozess werden auch viele Mineralien und Vitamine entfernt, sodass hauptsächlich Stärke zurückbleibt. Sobald die Giftstoffe ausgewaschen sind, können die Samen getrocknet, zu Pulver gemahlen und als Brei verzehrt werden.
Rosskastaniensamen enthalten bis zu 40 % Wasser, 8–11 % Protein und 8–26 % giftige Saponine, die ausgelaugt werden müssen, damit die Samen unbedenklich verzehrt werden können.
Amerikanische Indianer haben es getan auf die folgende Weise: Die Nüsse wurden langsam gebrannt (um die Saponine unschädlich zu machen) und dann, nachdem man sie in dünne Scheiben geschnitten hatte, in einen Stoffbeutel gegeben und darin gewaschen fließendes Wasser innerhalb von 2-5 Tagen. Allerdings ist es auch danach nicht empfehlenswert, größere Mengen Kastaniensamen zu verzehren.
Die Verwendung von Rosskastanie (gewöhnlich) in der Medizin
Rosskastanie wird als adstringierendes und entzündungshemmendes Mittel verwendet. Auch als Mittel zur Verbesserung des Tonus von Venenwänden, die durchhängen oder sich dehnen, was zu Venen- oder anderen Krankheiten führen kann. Es reduziert auch die Flüssigkeitsretention, indem es die Kapillarpermeabilität erhöht. Verengt die Blutgefäße und erhöht dadurch den Blutdruck. Fördert die Heilung.
Die Rinde der Rosskastanie wird als entzündungshemmendes, adstringierendes, harntreibendes, fiebersenkendes, tonisierendes und gefäßverengendes Mittel verwendet.
Wird in kleinen Dosen innerlich zur Behandlung einer Vielzahl von Erkrankungen eingesetzt Gefäßerkrankungen, einschließlich Arterien, Krampfadern, Venenentzündungen, Beingeschwüre, Hämorrhoiden und. Es ist auch in Lotionen und Gelen zur äußerlichen Anwendung enthalten.
Rosskastanienrindentee wird zur Behandlung von Ruhr und äußerlich zur Behandlung von Lupus und Hautgeschwüren eingesetzt. Aus den Blättern hergestellter Tee wird als Stärkungsmittel zur Behandlung von Fieber und Keuchhusten verwendet.
Aus Rosskastaniensamen gewonnenes Öl wurde äußerlich zur Behandlung von Rheuma eingesetzt.
Verwendete Teile: Rinde, die im Herbst gesammelt wird, ist der Rinde junger Zweige vorzuziehen. Manchmal im Frühjahr gesammelt und zur späteren Verwendung getrocknet. Kastaniensamen - Sperma Hippocastani.
Organoleptische Eigenschaften von Samen: Der Geruch ist leicht, der Geschmack ist bitter, scharf.
Vorbereitungen:„Eskuzan“ gegen Krampfadern, „Esflazid“ gegen Krampfadern und andere.
Verwendungen von Rosskastanie (häufig), die durch klinische Beweise gestützt werden: innerlich, zur Behandlung von Symptomen einer chronischen Veneninsuffizienz, einschließlich Schmerzen, Schweregefühl in den Beinen, nächtliches Gefühl usw. Äußerlich zur symptomatischen Behandlung chronischer Veneninsuffizienz, Verstauchungen etc.
In Arzneibüchern und Systemen beschriebene Verwendungen traditionelle Medizin: Behandlung .
Die Verwendung von Rosskastanie (gewöhnlich) in der Volksmedizin
Rosskastanie (häufig) wird in der Alternativmedizin als Analgetikum, Blutstillungsmittel und Wundheilmittel eingesetzt.
In der Volksmedizin beschriebene (häufige) Verwendungen von Rosskastanie, die nicht durch experimentelle oder klinische Daten gestützt werden: Behandlung von Bakterienruhr und Fieber. Auch als blutstillendes Mittel bei übermäßigem Menstruationsfluss oder anderen gynäkologischen Blutungen sowie als Tonikum.
Wirtschaftlicher Einsatz von Rosskastanie (üblich)
Der Samen enthält unterschiedliche Mengen an Saponinen. Aus Samen gewonnene Stärke kann zum Waschen (zum Festigen von Stoffen) verwendet werden.
Aus der Rinde der Rosskastanie wird ein gelber Farbstoff gewonnen. Die Blüten enthalten den gelben Antioxidansfarbstoff Quercetin.
Rosskastanienholz (normal) ist weich, leicht und nicht haltbar. Es hat einen geringen kommerziellen Wert und wird hauptsächlich zur Herstellung von Möbeln, Schmuckschatullen und Holzkohle verwendet.
Synonyme: Aesculus asplenifolia, Aesculus castanea, Aesculus memmingeri, Aesculus procera.

| Russisch: | Rosskastanie. | |
| Ukr. | Hydraulische Kastanie. | |
| Englisch: | Rosskastanie. | |
| Deutsch: | Gemein Rosskastanie. | |
| Französisch: | Marronier l'Inde. | |
| Die Pflanze erhielt ihren Namen aufgrund der entfernten Ähnlichkeit des Samens mit den Früchten der essbaren Kastanie – Castanea sativa Mill. (Buchenfamilie - Fagaceae), die in Westtranskaukasien wächst. Der wissenschaftliche Name der Pflanze wird aus dem Lateinischen als „Rosskastanien-Eiche“ übersetzt. | ||
Botanische Beschreibung
Ein hoher (bis zu 30 m) Laubbaum mit einer breiten, dichten Krone aus der Familie der Rosskastaniengewächse (Hippocastanaceae). Die Blätter sind gegenständig, lang gestielt, handförmig zusammengesetzt mit 5–7 sitzenden, obovaten, länglichen, spitzen Blättern. Die Blüten sind unregelmäßig, weiß mit rot-rosa Flecken und in aufrechten Pyramidenrispen gesammelt. Blüht im Mai. Die Frucht ist eine runde Kapsel mit einem Durchmesser von bis zu 6 cm, die mit großen, weichen Stacheln bedeckt ist und in deren Inneren sich 1–2 große, braun glänzende Samen befinden. Die Früchte reifen im September–Oktober.
Geografische Verteilung
IN Tierwelt als Reliktpflanze in den Bergwäldern der Balkanhalbinsel (Albanien, Griechenland, Jugoslawien) gefunden. Es wird seit dem 16. Jahrhundert in Europa und der Ukraine angebaut. in Gärten und Parks als Zierpflanze.
Medizinische Rohstoffe
MIT therapeutischer Zweck und aus der Rinde junger Zweige werden Medikamente hergestellt (Cortex Aesculi hippocastani), Blatt (Folium Aesculi hippocastani), Blumen (Flores Aesculi hippocastani) und Früchte (Fructus Aesculi hippocastani). Die Rinde wird im Frühjahr gesammelt, in Stücke geschnitten und sofort nach dem Sammeln an der frischen Luft oder an einem gut belüfteten Ort getrocknet. Die Blüten werden im Mai geerntet, am ersten Tag in der Sonne getrocknet und dann unter einem Baldachin oder im Innenbereich getrocknet. Die Blätter werden von Mai bis September geerntet, bis sie gelb werden, mit oder ohne Blattstiele. An der frischen Luft unter einem Baldachin oder an einem gut belüfteten Ort trocknen und in einer dünnen Schicht (2–3 cm) verteilen. Vollreife Früchte werden geerntet, wenn sie zu fallen beginnen. Trocknen Sie sie unter einem Baldachin oder an einem gut belüfteten Ort bei Temperaturen bis zu 25 °C.
Die offiziellen Rohstoffe in der Ukraine sind Kastanienblätter und -früchte.
In anderen europäischen Ländern zu erhalten Medikamente Auch die Rinde der Zweige, die Schale der Früchte und die Blüten der Pflanze werden verwendet.
Biologisch aktive Substanzen
Die pharmakologische Aktivität von Rosskastanienfrüchten hängt mit dem Gehalt des Cumaringlycosids Esculin (Esculosid) und seines Aglycons Esculetin (Escinol), des Oxycumaringlycosids Fraxin und seines Aglycons Fraxetin sowie des Triterpen-Saponinglykosids β-Amyrin-Typ Escin zusammen ( Gehalt bis zu 13%).
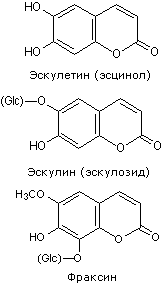
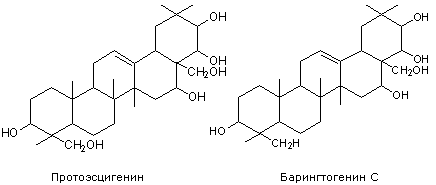
Weiter chemische Analyse zeigten, dass escin eine Mischung aus mehreren Substanzen ist: α-escin, β-escin und cryptoescin (H. Wagner et al., 1970), oder Aescine Ia, Ib, IIa, IIb und IIIa (N. Murakami et al., 1994), Aglykone davon sind Escigenin, Protoescigenin, Baringtogenine C und D.
Aescine IIIb, IV, V und VI, Isoescine Ia, Ib und V wurden auch in Rosskastanienfrüchten gefunden (M. Yoshikawa et al., 1998). Der Hauptbestandteil, der die biologische Aktivität von Escin bestimmt, ist β-Escin. Bei der Untersuchung des Arzneimittels Escin (hergestellt von JSC Galychfarm) mittels Flüssigkeitschromatographie wurde festgestellt, dass der Gehalt an β-Escin darin 76,35–79,29 % beträgt (A.V. Shovkovy und A.T. Shein, 1999). Kastanienfrüchte enthalten neben Aescin weitere Saponinglykoside. Insbesondere die saure Hydrolyse der Saponinfraktion ergab die Sapogenole Hypocaesculin (21-O-Angeloyl-22-O-Tigloyl-R1-Baringenol oder 21-O-Tigloyl-22-O-Angeloyl-R1-Baringenol) und Baryngtogenol-C -21 -angelat (T. Konoshima und K. H. Lee, 1986).

Die Aescine Ia, Ib, IIa und IIb wurden auch in japanischen Kastanienfrüchten identifiziert A. turbinata Blume (M. Yoshikawa et al., 1999).
Zusätzlich zu den bereits bekannten wurden in den Früchten der Chinesischen Kastanie Aesculus chinensis neue Triterpensaponine gefunden (X. W. Yang et al., 1999; J. Zhao et al., 2001):
Darüber hinaus enthalten die Früchte der Gemeinen Kastanie etwa 0,13 % Flavonoidglykoside (Quercitrin, Isoquercitrin, Quercetin und Kaempferol), etwa 0,9 % Gerbstoffe (Catechin-Tannin), fettes Öl (5–7 %), Proteine (11 %), Pektine , Stärke (bis zu 49,5 %).
Kastanienblüten und -blätter sind außerdem reich an Flavonoiden – Derivaten von Kaempferol und Quercetin. Konkret enthalten die Blätter Kaempferol-3-Glucosid, Kaempferol-3-Arabinosid, Kaempferol-3-Rhamnoglucosid, Quercitrin, Isoquercitrin, Rutin und Sireoside. Kastanienblüten enthalten neben Flavonglykosiden Schleim, Tannine und Pektinstoffe und Blätter Pektinstoffe und Carotinoide (Lutein, Violaxanthin).
Kastanienrinde enthält das Cumarin-Glykosid Äsculin (3 %) und sein Aglykon Äsculetin, Escin, die Oxycumarin-Glykoside Fraxin und Scopolin und deren Aglykone (Fraxetin und Scopoletin), das Flavonoid Quercetin, Tannine (insbesondere das Catechin-Dimer Proanthocyanidin-A2), Phytosterole (Stigmasterol, α-Spinasterol, β-Sitosterol), fettes Öl (2,5–7 %), Zucker (9 %), Askorbinsäure, Thiamin, Phyllochinon.
Geschichte der Verwendung in der Medizin
Die erste Erwähnung der Verwendung von Kastanien zu medizinischen Zwecken erfolgte im Jahr 1556. Der Arzt Peter Andreas Mattioli (1500–1577) empfahl, Pferden, die unter Atemnot litten, Rosskastanienfrüchte zu verabreichen. Im Jahr 1575 brachte der Botaniker Clausius Kastaniensämlinge aus der Türkei mit und pflanzte sie in Wien an Zierbäume. Im Jahr 1615 wurden Kastanien in Frankreich gepflanzt und 200 Jahre später tauchten sie auch in Amerika auf. Seit 1842 begann die Landschaftsgestaltung Kiews mit Kastanienbäumen. Einige Botaniker dieser Zeit glaubten, dass die Kastanie aus Indien stamme, worauf ihr französischer Name „Marronier d'Inde“ hinweist. Erst im 19. Jahrhundert. Es wurde festgestellt, dass der Geburtsort der Kastanie die Bergwälder der Balkanhalbinsel sind.
Die amerikanischen Indianer bereiteten aus den giftigen, auf heißen Steinen gerösteten Früchten der Rosskastanie ein Püree zu, legten es anschließend mehrere Tage lang in Limettenwasser ein und machten daraus Mehl. Aus dem gekeimten Samen, der durch die Umwandlung von Bitterstoffen in Süße schmackhaft wird, stellten sie Malz her. C. L. Millspaugh (1974) glaubt, dass die Indianer die Samenschale als verwendet haben narkotische Substanz(In Bezug auf die Aktivität entsprachen 10 g 3 g Opium). Pulver aus den Samen und zerkleinerten Zweigen wurde zur Vergiftung von Fischen verwendet.
In der Volksmedizin Südeuropas im 18.-19. Jahrhundert. Kastanienfrüchte und -rinde wurden als Ersatz für Chinarinde zur Behandlung von Malaria, fieberhaften Erkrankungen und Amöbenruhr verwendet. Besonders beliebt waren diese Heilmittel in Frankreich, was auf die politische Isolation des Landes während der Herrschaft Napoleons II. und die Einstellung der Einfuhr teurer Chinarinde zurückzuführen war. Historische Quellen zeigen jedoch, dass Kastanienheilmittel eine schwächere Wirkung hatten als Chinarinde. Später gab es Berichte, dass Kastanien einige Krankheiten behandeln, die mit einer Durchblutungsstörung einhergehen. Pulver aus der Frucht wurde auf Krampfadergeschwüre gestreut. Im Jahr 1708 berichtete Tabler über die Wirksamkeit des Suds bei der Behandlung von Hämorrhoiden. Seit 1866 tauchte in europäischen Apotheken Kastanientinktur auf, die bei chronischen Darmentzündungen, Gicht und Hämorrhoiden verschrieben wurde.
Die Rosskastanie wurde vom französischen Arzt A. Artault de Vevey in die wissenschaftliche und praktische Medizin eingeführt. 1896 in einer französischen Zeitschrift „Revue de théérap. meed. chirur.“ seine Veröffentlichungen erschienen ca erfolgreiche Behandlung Hämorrhoiden und Krampfadern mit Kastanientinktur. Der berühmte französische Kräuterkundler Leclerc betrachtete die Kastanie wirksame Mittel zur Behandlung von Prostatitis und Prostataadenom. In den 50er Jahren des 20. Jahrhunderts. In Deutschland begann die Produktion venotonischer Kastanienpräparate.
Kräuterpräparate aus der Rosskastanie werden auch heute noch in vielen Ländern häufig in der Volksmedizin eingesetzt. Kastanienblütentinktur hat entzündungshemmende und schmerzstillende Eigenschaften, der Samen hat entzündungshemmende Eigenschaften und die Samenschale hat blutstillende, entzündungshemmende und schmerzstillende Eigenschaften. Frischer Blumensaft wird oral gegen Krampfadern, Thrombophlebitis, Arteriosklerose und Hämorrhoiden verschrieben. Mit Alkohol konservierter Blütensaft, Tinktur aus Blüten oder Früchten werden oral und äußerlich bei Krampfadern und Hämorrhoiden sowie als Einreibung bei Arthritis, rheumatischen und Gichtschmerzen empfohlen. Bei Uterus- und Hämorrhoidalblutungen wird lokal eine Abkochung von Fruchtschalen verschrieben (Bäder, Spülungen). Kastaniensamenpulver wird bei Erkältungen und Atemwegserkrankungen eingesetzt.
Abkochungen und Aufgüsse aus Kastanienrinde haben adstringierende, blutstillende, entzündungshemmende, schmerzstillende und krampflösende Eigenschaften. Sie werden als wirksame innere und äußere Heilmittel bei anhaltendem Durchfall, chronischer Kolitis, erhöhtem Säuregehalt des Magensaftes, Erkrankungen der Atemwege (chronische Bronchitis) und Malaria eingesetzt. Sie werden als blutstillendes Mittel bei Hämorrhoiden und inneren Blutungen, insbesondere bei Uterusblutungen, empfohlen.
Aufgüsse aus Rinde, Tinktur aus Früchten, Aufgüsse aus Fruchtschalen und frisch geriebenen Kastanienblättern werden auch als äußeres Heilmittel zur Versorgung eiternder Wunden verwendet.
Pharmakologische Eigenschaften
Eine Untersuchung der pharmakologischen Aktivität von Kastanienkräuterpräparaten (alkoholischer Extrakt, alkoholische Tinkturen, Abkochungen und Aufgüsse aus Blättern, Blüten und Früchten) zeigte, dass der alkoholische Extrakt der Frucht am wirksamsten ist, der eine geringe akute Toxizität aufweist.
Kastanienfruchtextrakt stimuliert die Herztätigkeit bei Kaltblütern, senkt den Blutdruck bei Katzen um 15–70 %, erweitert in kleinen Dosen die Gefäße des isolierten Ohrs eines Kaninchens und verengt sie in höheren Dosen. Bei experimenteller Thrombophlebitis bei Hunden reduziert Kastanienextrakt die allgemeine Entzündungsreaktion und die lokale Schwellung. Bei Menschen ohne Pathologie der peripheren Blutgefäße wurde festgestellt, dass der Fruchtextrakt den Tonus der Unterschenkelvenen erhöht.
Darüber hinaus weist es entzündungshemmende, abschwellende, schmerzstillende und kapillarstärkende Eigenschaften auf, verringert die Blutviskosität und verhindert die Entstehung von Stauungen in den Kapillaren.
Der gereinigte Gesamtextrakt aus Rosskastanienfrüchten fördert die umgekehrte Entwicklung der experimentellen Cholesterin-Atherosklerose bei Kaninchen, normalisiert den Gehalt an Cholesterin und Lecithin im Blut und reduziert die Lipoidose der Aorta und der Leber.
Die pharmakologische Aktivität von Rosskastanien-Kräuterpräparaten hängt hauptsächlich mit dem Gehalt des Triterpen-Saponinglykosids Escin und seiner Derivate zusammen. Wie andere Saponine hat Aescin eine hämolytische Aktivität, die sich jedoch in therapeutischen Dosen nicht manifestiert. Im Gegensatz zur kristallinen β-Escinsäure, die in Wasser nahezu unlöslich ist, werden die wasserlöslichen Aescinsäureformen von α-Escinsäure, Natrium-α-Escinat und amorphe β-Escinsäure gut aus dem Magen-Darm-Trakt resorbiert. Natrium-β-Escinat und amorphe β-Escinsäure haben bei oraler Verabreichung und Aescin bei subkutaner Verabreichung ausgeprägte entzündungshemmende und antiödematöse Eigenschaften und verbessern den Gewebetrophismus bei unzureichender Blutversorgung und Ödemen.
Die entzündungshemmenden Eigenschaften von Aescin und seinen Derivaten wurden in zahlreichen Experimenten bestätigt verschiedene Modelle Entzündung. Sie hemmen die Entwicklung experimenteller Schwellungen der Pfoten von Ratten, die durch Ovalbumin, Histamin, Serotonin, Verbrennungen oder Stagnation (Lymphödem), Anwendung lokal reizender Substanzen (Chloroform) verursacht werden. Escin verringert sich dosisabhängig (um maximal 70 %). die Durchlässigkeit der Plasma-Lymph-Schranke, die durch die Injektion von Bradykinin in die Pfote von Kaninchen verursacht wird (M. Rothkopf und G. Vogel, 1976), verhindert das Auftreten einer exsudativen Reaktion auf die Verabreichung der Prostaglandine E1 und F2a (M. Rothkopf-Ischebeck und G. Vogel, 1980; D. Longiave und al., 1978). Eine ähnliche Wirkung von Aescin tritt in Modellen für ultraviolettes Erythem auf (R. Eisenburger et al., 1976), Entzündung der Schleimhaut Blase Ratten, induziert durch Elektrokoagulation (P. Strohmenger und H. Wenzel, 1976), postischämisches Muskelödem und Hirnödem aufgrund einer Kälteverletzung (M. Arnold und M. Przerwa, 1976). Escin hemmt dosisabhängig die Entwicklung einer Formalinperitonitis und einer Carrageenan-Pleuritis bei Ratten (Rothkopf und G. Vogel, 1976; M. Guillaume und F. Padioleau, 1994); reduziert die Menge des Exsudats, seinen Proteingehalt und die Migration von Leukozyten in die Pleurahöhle. Es wurde festgestellt, dass mit einer Erhöhung der Aescin-Dosis die Exsudation kleiner Moleküle in die Bauchhöhle im Vergleich zu großen Molekülen wirksamer gehemmt wird.
Die Fähigkeit gereinigter Präparate der Aescine Ia, Ib, IIa und IIb in einer Dosis von 50–200 mg/kg, das anfängliche exsudative Stadium der Entzündung zu unterdrücken, wurde von H. Matsuda et al. bestätigt. (1997) zu verschiedenen experimentellen Modellen: Entzündung der Haut von Ratten und Mäusen als Reaktion auf die Einführung von Essigsäure, Ovalbumin, Dextran, Trypsin, Hyaluronidase, Kaolin, Bienengift, Carrageenin, Histamin, Bradykinin und die Arthus-Reaktion. Aescine verhindern mit Ausnahme von Aescin Ia die Erhöhung der Gefäßpermeabilität unter dem Einfluss von Serotonin. In Modellen der späten (proliferativen) Phase der Entzündung wurde kein Effekt beobachtet. Andere Forscher weisen jedoch auf die Fähigkeit von Aescin und seinen Hydrolyseprodukten hin, die Entwicklung von Wattegranulomen bei Ratten zu hemmen (R. Eisenburger et al., 1976), eine Reaktion auf die Implantation von Kunststoffschaum (M. Guillaume und F. Padioleau, 1994; M. Przerwa und M. Arnold, 1975).
Von großer Bedeutung für die Entwicklung der antiexsudativen Wirkung von Aescin ist seine Fähigkeit, den Gefäßwiderstand zu erhöhen, was in verschiedenen Entzündungsmodellen im Evans-Blau-Test (Rothkopf und G. Vogel, 1976) sowie durch die Ergebnisse nachgewiesen wurde eines Petechientests bei Meerschweinchen, die eine skorbutogene Diät erhielten. Escine, insbesondere das Sapogenin Escinol, hemmen die Hyaluronidase-Aktivität (IC50 149,9 µM bzw. 1,65 µM). (R. M. Facino et al., 1995). Die Grundlage der entzündungshemmenden Wirkung von Aescin ist somit die Stärkung der Kapillarwände. Escin reduziert die Anzahl der Poren in den Wänden der Kapillaren und deren Durchmesser. In Tierversuchen wurde festgestellt, dass Aescin eine 600-mal stärkere antiexsudative Wirkung hat als das klassische Flavon Rutin. Wie in Modellen der Formaldehyd-Peritonitis, der experimentellen Pleuritis bei Ratten und der Schwellung der Kaninchenpfote gezeigt wurde, ist das antiexsudative Potenzial von Aescin mit der Wirkung von Acetylsalicylsäure, Hydrocortison, Phenylbutazon und Butadion vergleichbar und übertrifft diese in einigen Fällen sogar. Es besteht die Vermutung, dass die entzündungshemmende Wirkung von Aescin mit seiner Wirkung auf die Nebennierenrinde und der Fähigkeit, die Sekretion von Glukokortikoiden zu stimulieren, zusammenhängt.
Escin hat ausgeprägte membranotrope Eigenschaften. Durch die Bindung an die Lipide biologischer Membranen erhöht es die Fließfähigkeit der Lipiddoppelschicht (L. V. Ivanov et al., 1988). Bedenkt man, dass Aescin wesentlich stärker an die Membranen von Erythrozyten und Gefäßwandzellen bindet als an Liposomen (die aus Phospholipiden bestehen), kann man auch von einer Fähigkeit ausgehen, mit Membranproteinen zu reagieren. Eine solche Wechselwirkung ist zwischen dem Glucuronsäurerest und den Aminosäureresten von Lysin und Arginin möglich. Experimente zur Untersuchung der Fließfähigkeit von Lipiden in der Gefäßwand weisen darauf hin, dass der Anstieg des Gefäßwiderstands in Gegenwart von Aescin auf einer Erhöhung ihrer Elastizität beruht und nicht mit einer Verdichtung des Gefäßgewebes verbunden ist. Die Erhöhung der Lipidflüssigkeit erklärt teilweise die vasotonisierende Wirkung des Arzneimittels. Die membranstabilisierende Wirkung von Escinol, Escin und Esculosid wurde in Experimenten zur Untersuchung der Resistenz von Erythrozyten gegenüber osmotischer Hämolyse nachgewiesen. Die optimale aktive Konzentration von Aescin von 10-5 G entsprach dem Arzneimittelspiegel im Blut von Patienten nach Einnahme einer therapeutischen Dosis (L.A. Chaika und I.I. Khadzhai, 1977). Als Saponin reduziert Escin die Oberflächenspannung der Flüssigkeit, wird gut an der Grenzfläche der Oberflächen adsorbiert und diese Wirkung erstreckt sich auf die Gefäßwand. Escin erhöht die Benetzbarkeit der Kapillaren, was den Fluss der Gewebeflüssigkeit in die Kapillare erleichtert. Dadurch wird die Flüssigkeit, die das perivaskuläre Ödem vorwegnimmt, aufgrund des erhöhten onkotischen Drucks in den Kapillaren in die Gefäße geleitet.
Wichtige Mechanismen der entzündungshemmenden und antiödematösen Wirkung von Aescin sind auch seine venotonische Wirkung. Die ausgeprägten venotonischen Eigenschaften von Aescin wurden in experimentellen In-vitro-Studien an der Pfortader und der Vena saphena von Kaninchen, der Vena saphena bei Hunden sowie an Abschnitten der normalen und varikösen Vena bestätigt. saphena human (EC50 9,4–15,9 µM/l). In einer Studie an normalen und leicht erweiterten Venen mit Klappeninsuffizienz betrug der erzielte Effekt 70–71 % der maximal möglichen Kontraktion unter dem Einfluss von KCl und 43 % der Kontraktion aufgrund von Noradrenalin. Allerdings reagierten Venen, die tief von Krampfadern betroffen waren, schwächer auf Aescin – die venotonische Wirkung betrug nur 10 % des maximal möglichen (F. Brunner et al., 2001). Diese Ergebnisse bestätigen die größere therapeutische Wirksamkeit von Aescin im Frühstadium von Krampfadern. Die venotonische Wirkung von Escin bei der Untersuchung von Abschnitten normaler menschlicher Vena saphena hielt eine Stunde nach Entfernung des Arzneimittels aus dem Inkubationsmedium an.
Von maximale Wirkung Escin war Acetylcholin und Vasopressin überlegen und hatte die gleiche Aktivität wie Serotonin und Dihydroergotamin. Allerdings ist die Affinität der Venenwand zu Aescin im Vergleich zu den aufgeführten Venotonika geringer, was auf eine nicht reversible Venenerweiterung unter dem Einfluss von Aescin hinweist (F. Annoni et al., 1979). An der perfundierten Vena saphena von Hunden hält die venotonische Wirkung von Aescin mehr als 5 Stunden an; das Medikament hat einen Anstieg des Venendrucks vorherbestimmt und auch die kontraktile Wirkung von Noradrenalin deutlich verstärkt. In-vivo-Studien an Hunden zeigen eine Verbesserung der Elastizität der Oberschenkelvene (M. Guillaume und F. Padioleau, 1994). Es wird angenommen, dass die venotonische Wirkung von Aescin auf der Stimulierung der Synthese und Freisetzung von Prostaglandin F2a in der Venenwand beruht. Wenn jedoch isolierte Rattenlungen mit einer Lösung, die Aescin enthält, perfundiert werden, erhöht sich die Freisetzung dieses Prostaglandins (F. Berti et al., 1977). Die ausgeprägte Wirkung von Aescin auf den Prozess des dichten Verschlusses der Venenklappen ist wichtig für die Verbesserung der Venenzirkulation und die Verhinderung von Reflux. Durch die Verwendung von Aescin können Sie eine Wirkung erzielen, die 90 % des maximal Möglichen durch die Wirkung von Noradrenalin beträgt.
Die Erhöhung des Venentonus erleichtert den Rückfluss des Blutes vom Gewebe zum Herzen und verbessert den Lymphfluss durch den thorakalen Lymphgang um 70 %. Darüber hinaus sinkt bei intravenöser Gabe von Aescin der Adrenalingehalt in den Nebennieren und der Blutdruck steigt, bei Perfusion isolierter Nebennieren wird eine vasokonstriktorische Wirkung beobachtet. Offensichtlich trägt die Kombination dieser Effekte auch zur Manifestation der antiödematösen Wirkung von Aescin bei.
Die venotonische und entzündungshemmende Wirkung von Aescin sorgt für seine therapeutische Wirkung bei Krampfadern. Bei der Entstehung von Krampfadern spielt nicht nur die venöse Stauung eine wichtige Rolle, sondern auch die Aktivierung von Endothelzellen unter hypoxischen Bedingungen. Am Modell Ex-vivo Eine isolierte menschliche Nabelvene, die unter Hypoxie perfundiert wurde, zeigte, dass Aescin zwei wichtige Ereignisse hemmt, die Voraussetzungen für die Aktivierung von Endothelzellen während Hypoxie sind. Es wirkt der Abnahme des ATP-Gehalts in Endothelzellen und der anschließenden Aktivierung von Phospholipase A2 entgegen, einem Enzym, das für die Freisetzung des Vorläufers des Plättchenaktivierungsfaktors (PAF) aus Zellmembranen sorgt Arachidonsäure- ein Vorläufer von Entzündungsmodulatoren - Leukotrienen und Prostaglandinen. Mittels Rasterelektronenmikroskopie wurde die Hemmung der Adhäsion von Neutrophilen und neutrophilenähnlichen Zellen der HL60-Linie an der Venenwand in Gegenwart von Aescin nachgewiesen. Die Hemmung der hypoxischen Aktivierung von Endothelzellen der Venenwand manifestierte sich bei einer Aescin-Konzentration von 100 ng/ml und erreichte ein Maximum bei einer Konzentration von 750 ng/ml (T. Arnould et al., 1996). Gleichzeitig nahm die Produktion von Superoxidanionen und Leukotrien B4 im System ab (C. Bougelet et al., 1998). Die antiradikalen Eigenschaften von Aescin wurden von anderen Forschern bestätigt – es hemmte dosisabhängig die enzymatische und nichtenzymatische Lipidperoxidation in vitro(EC 5–500 µg/ml) (M. Guillaume und F. Padioleau, 1994). Somit deuten die obigen Ergebnisse experimenteller Studien darauf hin, dass Aescin die durch Hypoxie induzierte Aktivierung von Endothelzellen hemmt, was zu einer erhöhten Adhäsion von Neutrophilen führt, und dass ihre Mediatoren und Proteasen zur Zerstörung der interzellulären Matrix beitragen und Schäden an der Venenwand verursachen mikroskopisch erinnern sie an die bei Krampfadern beobachteten Veränderungen. Indem es die Manifestationen von Entzündungen und Schäden an der Venenwand reduziert, hemmt Aescin die Freisetzung von Wachstumsfaktoren durch aktivierte Zellen, die an der proliferativen Phase der Entzündung beteiligt sind und zur Aufrechterhaltung der Veneninsuffizienz und zur Entwicklung von Krampfadern beitragen (R. W. Frick, 2000). ). Escin hält das Endothel unter Bedingungen venöser Stauung in einem intakten Zustand, verhindert die Rekrutierung, Adhäsion und Aktivierung von Neutrophilen, wirkt als Antagonist von Entzündungsmediatoren und verhindert so eine Schädigung der Venenwand. Diese Daten sowie die Ergebnisse der Untersuchung der venotonischen Aktivität unterstreichen einmal mehr den besonderen Wert der präventiven Anwendung von Aescin-Präparaten im Frühstadium von Krampfadern.
Es ist wichtig, dass andere biologisch aktive Substanzen, die in Gesamtextrakten der Kastanie enthalten sind, die entzündungshemmende Wirkung von Aescin verstärken. Somit erhöht sich in Gegenwart des natürlichen Flavonoidkomplexes der Kastanie (1:10) die Aktivität von Aescin um das Fünffache. Erdölextrakt aus Kastanienrinde hat zudem entzündungshemmende Eigenschaften. (F. Senatore et al., 1989).
Die antiexsudativen und kapillarstärkenden Eigenschaften von Aescin ermöglichen den Einsatz bei Hirnödemen, was erstmals 1967 von S. Gorini und R. Caponi bei Tieren mit Hirnödem aufgrund einer Kraniotomie experimentell nachgewiesen wurde. Weitere experimentelle Studien bestätigten die Wirksamkeit des Arzneimittels bei traumatischen Hirnödemen. (T. Tzonos und H. Riebeling, 1968; L. Auer, 1975) und ischämisch (M. Cerisoli et al., 1981) Genesis. Traumatische Hirnverletzungen sind durch ein vasogenes Hirnödem gekennzeichnet, das auf einer erhöhten Gefäßpermeabilität beruht.
In Zukunft wird es durch zytotoxische Ödeme verschlimmert – Schwellungen des Hirngewebes, die auf Stoffwechselstörungen beruhen, die durch den traumatischen Faktor selbst, vasogene Hirnödeme und die toxische Wirkung von Gewebeabbauprodukten verursacht werden. Die langsame Resorption von Blut aus dem Gehirngewebe und der Schädelhöhle fördert die Ansammlung von unteroxidierten und toxischen Gewebeabbauprodukten und erhöht so die Osmolarität und Hydratation (Ödeme und Schwellungen) sowohl lokal an der Verletzungsstelle als auch im gesamten Gehirn. Diese Prozesse führen zu einer Zunahme der Läsion, der Entwicklung oder Zunahme einer intrakraniellen Hypertonie, Kompression und Verschiebung des Gehirns. Hirnödeme und intrakranielle Hypertonie gehen immer mit einer Abnahme des Venentonus, einer Beeinträchtigung des venösen Abflusses, einer Stagnation des venösen Blutes in der Schädelhöhle mit der Entwicklung einer venösen Hypertonie einher, was zur Entwicklung eines destruktiven Ödems beiträgt. Durch die Wiederherstellung der beschädigten Gefäßpermeabilität und die Erhöhung des Venentonus verhindert Aescin die Entwicklung oder Beseitigung von Störungen des venösen Abflusses, venöser Hypertonie und Hirnödemen. Die Verringerung des Phänomens des Hirnödems und die Verbesserung des venösen Abflusses tragen außerdem zur Normalisierung der Hirndurchblutung bei, was wiederum zu einer Verbesserung der Durchblutung führt Bevorzugte Umstände zur schnellen Auflösung (Resorption) des Herdes von Gehirnkontusionen und Hämatomen. Durch die Beseitigung von Störungen der Durchlässigkeit der Gefäßwand und die Erhöhung des Venentonus sowie die Beseitigung von Ödemen verschiedener Gehirnstrukturen verhindert Aescin die Entwicklung pathophysiologischer Mechanismen, die den Schmerzreizen zugrunde liegen, erheblich und entfaltet somit eine analgetische Wirkung.
Die Aescine Ia, Ib, IIa und IIb verstärken die Evakuierungsfunktion des Magens von Mäusen (H. Matsuda et al., 2000), hemmen (insbesondere Aescins IIa und IIb) die Aufnahme von Alkohol im Magen-Darm-Trakt von Ratten (N. Murakami und I. Kitagawa, 1994).
Bei oraler Verabreichung an Mäuse (10–50 mg/kg) hemmen die Aescine Ia, Ib, IIa und IIb deutlich die Entwicklung von Ethanol-Magenschäden (H. Matsuda et al., 1999). Die gastroprotektive Wirkung von Aescinen wird unterdrückt, wenn Tieren zusätzlich Capsaicin (das afferente autonome Nervenfasern blockiert), N(G)-Nitro-L-Argininmethylester (NO-Synthase-Inhibitor) und Indomethacin (ein Inhibitor der Prostaglandinsynthese) verabreicht werden wie bei Tieren mit Streptozocin-Diabetes (mit abnormaler sympathischer Aktivität). nervöses System). Deacylierte Escin-Derivate sind in dieser Hinsicht nicht aktiv. Im perfundierten Magen anästhesierter Ratten wurde die Fähigkeit von Aescin (in Dosen von 10 und 50 mg/kg) nachgewiesen, die durch Histamin und Carbachol stimulierte Sekretion von Salzsäure zu hemmen. (E. Marhuenda et al., 1994). E. Marhuenda et al. (1994) Beachten Sie, dass Indomethacin die Wirkung von Aescin auf die Schädigung der Magenschleimhaut durch Ethanol neutralisiert, sie konnten jedoch keinen Anstieg der Produktion von Prostaglandin E2 feststellen. Daher sind die Mechanismen der gastroprotektiven Wirkung von Aescin noch nicht vollständig aufgeklärt. Offenbar ist dies zum Teil auf die antisekretorische Aktivität des Arzneimittels zurückzuführen und wird zum Teil durch endogene Prostaglandine, Stickstoffmonoxid, Capsaicin-empfindliche afferente Neuronen und das sympathische Nervensystem vermittelt.
Die Escine Ia, Ib, IIa und IIb zeigen im Tierversuch mit oraler Glukosebelastung hypoglykämische Wirkungen (N. Murakami und I. Kitagawa, 1994; M. Yoshikawa et al., 1996). Bei normalen Tieren sowie bei intraperitonealer Verabreichung von Glukose wird die hypoglykämische Wirkung von Aescins nicht beobachtet. Es wurde festgestellt, dass die Escine Ia und IIa keine insulinähnliche Aktivität haben und die Insulinproduktion nicht stimulieren können. Ihre blutzuckersenkende Wirkung ist mit einer Hemmung der Glukoseaufnahme im Dünndarm verbunden (H. Matsuda et al., 1998).
Esculosid (Esculin) stabilisiert aufgrund der Hemmung der Hyaluronidase-Aktivität die Kapillaren, stimuliert die antithrombotische Aktivität des Blutserums und blockiert die Hemmung der Antithrombinsynthese durch Zellen des retikuloendothelialen Systems. Escin verbessert auch die rheologischen Eigenschaften von Blut. Dadurch fördern Rosskastanienpräparate den venösen Abfluss, verbessern die Mikrozirkulation, wirken der Entstehung von Kapillarstauungen entgegen und wirken sich positiv auf den Gewebetrophismus aus. Durch die Normalisierung des Gleichgewichts zwischen intravaskulärem Druck und Festigkeit der Gefäßwand wird das Auftreten von Blutungen verhindert.
Auch die gerinnungshemmende Wirkung von Rosskastanienpräparaten wird mit Fraxin in Verbindung gebracht. Aber im Allgemeinen sind sie in Bezug auf die gerinnungshemmenden Eigenschaften Dicumarin unterlegen.
In Experimenten in vitro Aescin in einer Konzentration von mehr als 10 μg/ml verkürzt die Kristallisationsdauer der Harnsäure erheblich. In Experimenten an Ratten zeigte Esculosid eine mäßige saluretische Aktivität und erhöhte dosisabhängig die renale Ausscheidung von Chloriden, Natrium und Kalium. Die diuretische Wirkung von Aescin ist viel schwächer; bei der höchsten untersuchten Dosis wird die minimale Wirkung von Aesculosid erreicht (M. J. Martin et al., 1990).
Das Experiment zeigte eine schwache krampflösende (Papaverin-ähnliche) Wirkung von Äsculetin, Äsculin, Fraxin und Fraxetin auf die glatte Muskulatur innerer Organe und Herzkranzgefäße.
Experimente an Ratten weisen darauf hin, dass das Catechin-Dimer Proanthocyanidin-A2 der Kastanienrinde den Trophismus verbessert Skelettmuskeln normal und nach ihrer traumatischen Denervierung (P. Ambrogini et al., 1995).
Es gibt Hinweise darauf, dass Saponine (insbesondere Aesculetin) und Verbindungen der Peptidnatur von Kastanienfrüchten das Wachstum einiger Bakterien und Pilze hemmen. Die Aescine IVc, IVd, IVe und IVf aus dem Samen von Aesculus chinensis besitzen Eigenschaften als Inhibitoren der BOL-1-Protease (X. W. Yang et al., 1999).
Kastanienextrakt hemmt bei intraperitonealer Verabreichung das Wachstum von Ehrlich-Asziteskarzinomen und Lymphosarkomen 150, die Mäusen implantiert wurden, und bei Untersuchungen an einem Hühnerembryo das Wachstum von Lymphosarkomen und C3H-Karzinomen. Es wurde festgestellt, dass es keine antimitotische Wirkung hat, aber nach einer kurzen Inkubation mit Tumorzellen (für 30 Sekunden) verursacht es in diesen irreversible morphologische Veränderungen. Es wurde festgestellt, dass die Antitumoreigenschaften des Kastanienextrakts gegen Zellen der KB-Linie mit der Saponinfraktion zusammenhängen, insbesondere mit den Sapogenolen Hypocaesculin und Barynthogenol-C-21-Angelat, die durch dessen saure Hydrolyse gewonnen werden (T. Konoshima und K. H. Lee, 1986).
Bei lokale Anwendung(kutan) Aescin und markiertes Natrium-3H-Escinat haben in Experimenten an Mäusen, Ratten und Schweinen gezeigt, dass es schnell in benachbarte Haut- und Muskelbereiche eindringt. Die Resorption von Aescin in innere Organe, Blut, Urin, Haut und Muskeln anderer Bereiche ist begrenzt. Die Konzentration von markiertem Aescin ist in der Dermis 50–600-fach und in den Muskeln 10–50-fach höher als im Blut. Nur 0,5–1 % des Aescins werden innerhalb von 24 Stunden mit dem Urin ausgeschieden. Es wird geschätzt, dass die Gesamtausscheidung des Arzneimittels im Urin und in der Galle 1–2,5 % der verabreichten Dosis beträgt (W. Lang, 1977). Bei intravenöser Verabreichung wird Aescin schnell mit Urin und Galle aus dem Körper ausgeschieden orale Verabreichung relativ schnell hauptsächlich aus dem Zwölffingerdarm resorbiert.
Um die Bioverfügbarkeit und Pharmakokinetik seiner Präparate zu untersuchen, wurden Methoden für den Radioimmun- und Enzymimmunoassay der Escin-Konzentration im Blutserum entwickelt (T. Lehtola und A. Huhtikangas, 1990; C. Hentschel et al., 1994).
